Tofacitinib citrát je liek na predpis (obchodný názov Xeljanz) pôvodne vyvinutý spoločnosťou Pfizer pre triedu perorálnych inhibítorov Janus kinázy (JAK). Môže selektívne inhibovať JAK kinázu, blokovať dráhy JAK/STAT, a tým inhibovať transdukciu bunkového signálu a expresiu a aktiváciu súvisiaceho génu, používanú na liečbu reumatoidnej artritídy, psoriatickej artritídy, ulceróznej kolitídy a iných imunitných ochorení.
Liečivo obsahuje tri dávkové formy: tablety, tablety s predĺženým uvoľňovaním a perorálne roztoky. Jeho tablety boli prvýkrát schválené FDA v roku 2012 a lieková forma s predĺženým uvoľňovaním bola schválená FDA vo februári 2016. Ide o prvú liečbu reumatoidných kĺbov. Yan je inhibítor JAK užívaný perorálne raz denne. V decembri 2019 bola opäť schválená nová indikácia pre lieky s predĺženým uvoľňovaním pre stredne závažnú až závažnú aktívnu ulceróznu kolitídu (UC). Okrem toho bola dokončená súčasná 3. fáza klinických skúšok pre ložiskovú psoriázu a prebieha ďalších šesť klinických skúšok 3. fázy, ktoré zahŕňajú aktívnu psoriatickú artritídu, juvenilnú idiopatickú artritídu atď. Druhy indikácií. Výhody tabliet s predĺženým uvoľňovaním, ktoré majú dlhodobý účinok a stačí ich užívať raz denne, prispievajú k zvládaniu a kontrole chorôb pacientov.
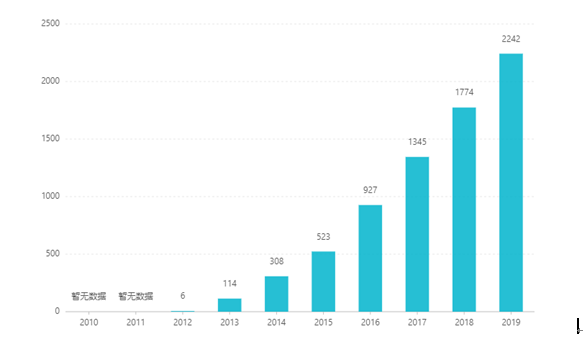
Od zaradenia na burzu sa jej tržby z roka na rok zvyšovali a v roku 2019 dosiahli 2,242 miliardy USD. V Číne bola tabletová lieková forma schválená na uvedenie na trh v marci 2017 a v roku 2019 vstúpila do katalógu zdravotného poistenia kategórie B. Najnovšie víťazné ponuka je 26,79 RMB. Kvôli vysokým technickým prekážkam prípravkov s predĺženým uvoľňovaním však táto lieková forma ešte nebola v Číne uvedená na trh.
JAK kináza hrá dôležitú úlohu pri zápaloch a ukázalo sa, že jej inhibítory liečia niektoré zápalové a autoimunitné ochorenia. Doteraz bolo celosvetovo schválených 7 inhibítorov JAK, vrátane Delgocitinibu od Leo Pharma, Fedratinibu od Celgene, upatinibu od AbbVie, Pefitinibu od Astellas, Baritinibu od Eli Lilly a Rokotinibu od Novartisu. Z vyššie uvedených liekov sú však v Číne schválené iba tofacitinib, baritinib a rokotinib. Tešíme sa, že „tablety s predĺženým uvoľňovaním citrátu tofatibu“ od spoločnosti Qilu budú schválené čo najskôr a budú prínosom pre viac pacientov.
V Číne pôvodný výskum tofacitib citrát schválila NMPA v marci 2017 na liečbu dospelých pacientov s RA s nedostatočnou účinnosťou alebo intoleranciou metotrexátu pod obchodným názvom Shangjie. Podľa údajov z Meinenetu bol predaj tabliet tofacitib citrátu v čínskych verejných zdravotníckych inštitúciách v roku 2018 8,34 milióna juanov, čo bolo oveľa menej ako jeho celosvetový predaj. Veľkú časť dôvodu tvorí cena. Uvádza sa, že počiatočná maloobchodná cena Shangjie bola 2 085 juanov (5 mg*28 tabliet) a mesačné náklady boli 4 170 juanov, čo nie je pre bežné rodiny malá záťaž.
Je však potrebné osláviť, že tofacitib bol po rokovaniach v novembri 2019 zaradený Národnou správou zdravotného poistenia do zoznamu „národného základného zdravotného poistenia, poistenia pracovného úrazu a poistenia v materstve“ na rok 2019. Uvádza sa, že mesačný poplatok bude znížený na menej ako 2 000 juanov po dohodnutí zníženia ceny, čo výrazne zlepší dostupnosť lieku.
V auguste 2018 komisia pre opätovné preskúmanie patentov Štátneho úradu pre duševné vlastníctvo vydala rozhodnutie o preskúmaní č. 36902 so žiadosťou o zrušenie platnosti a vyhlásila za neplatný hlavný patent spoločnosti Pfizertofatib, zložený patent, z dôvodu nedostatočného zverejnenia špecifikácie. Platnosť patentu na kryštalickú formu Pfizertofatiibu (ZL02823587.8, CN1325498C, dátum prihlášky 25.11.2002) však vyprší v roku 2022.
Databáza Insight ukazuje, že okrem pôvodného výskumu, päť generických liekov Chia Tai Tianqing, Qilu, Kelun, Yangtze River a Nanjing Chia Tai Tianqing bolo schválených na uvedenie na trh v domácich formuláciách tabliet tofacitinibu. V prípade typu tabliet s predĺženým uvoľňovaním však 26. mája predložila žiadosť o uvedenie na trh iba spoločnosť Pfizer z pôvodného výskumu. Qilu je prvou domácou spoločnosťou, ktorá podala žiadosť o uvedenie na trh pre túto formuláciu. Okrem toho je CSPC Ouyi v skúšobnej fáze BE.
Changzhou Pharmaceutical Factory (CPF) je popredným farmaceutickým výrobcom API, hotových formulácií v Číne, ktorá sa nachádza v Changzhou, provincia Jiangsu. CPF boli založené v roku 1949. Tofacitinib citrátu sme sa venovali od roku 2013 a už sme predložili DMF. Zaregistrovali sme sa v mnohých krajinách a môžeme vám poskytnúť najlepšiu podporu dokumentov pre tofacitinib citrát.
Čas odoslania: 23. júla 2021